Химический состав клетки
Клетки состоят из неорганических и органических веществ.
Знакомство с химическим составом клетки мы начнем с ВОДЫ.
В выражении «вода — основа жизни» нет никакого преувеличения. Биологическое значение воды огромно.
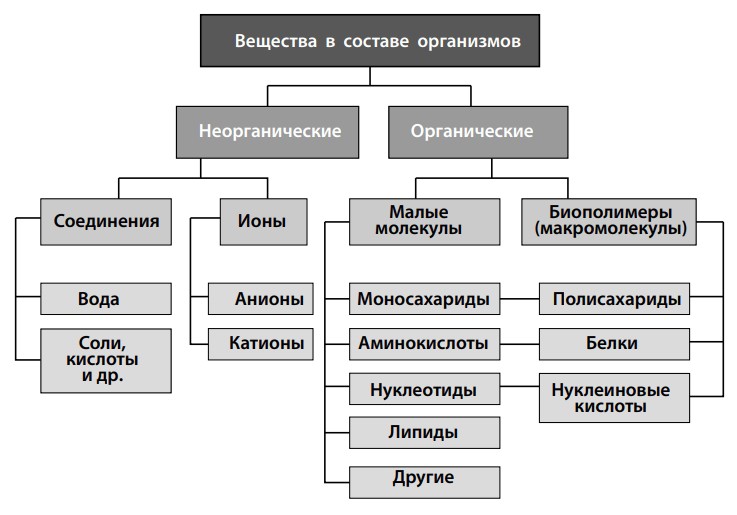
Вода:
- является основой внутренней среды организмов и внутриклеточной среды;
- обеспечивает транспорт веществ в клетках и организмах;
- обеспечивает поддержание пространственной структуры клетки;
- служит растворителем для многих веществ, средой для диффузии и химических реакций;
- участвует в реакциях фотосинтеза и гидролиза, а также во множестве других клеточных реакций;
- способствует равномерному распределению тепла в организме и участвует в терморегуляции (испарение пота);
- является средой обитания для многих организмов;
- способствует миграциям и распространению семян, плодов, личиночных стадий организмов;
- является средой, в которой происходит оплодотворение и др.
В организме человека примерно 60% воды, ее содержание больше, чем содержание всех других веществ вместе взятых. Большинство клеток живых организмов содержат 70-80% воды, в костных клетках ее около 20%, а в зубной эмали, самой твердой ткани организма — 10%.
Вспомните, что по отношению к способности растворяться в воде различают хорошо растворимые гидрофильные вещества и практически нерастворимые гидрофобные.
Кислород, как активный окислитель, участвует во многих химических процессах, происходящих в клетках. Углекислый газ является одним из конечных продуктов метаболизма. Количество минеральных солей, содержащихся в клетке, весьма мало, но без них нельзя обойтись, потому что они нужны для нормальной жизнедеятельности.
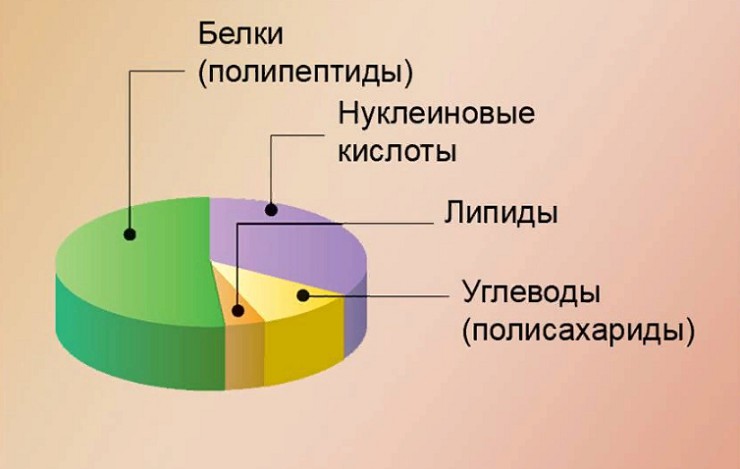
Органические вещества клетки представлены молекулами нуклеиновых кислот, белков, липидов (жиров и жироподобных веществ) и углеводов.
УГЛЕВОДЫ содержатся в каждой живой клетке без исключения. Особенно их много в клетках растений. В листьях, семенах, клубнях, плодах углеводы составляют до 90 % сухого остатка. В животных клетках углеводов содержится значительно меньше — около 1 % сухого остатка, за исключением клеток печени и мышц (до 5 %).
Углеводы разделяют на три основных класса соединений: моносахариды, олигосахариды и полисахариды.
Моносахариды или простые углеводы содержат в своих молекулах до семи атомов углерода, в зависимости от числа которых подразделяются на триозы (3 атомов), тетрозы (4 атомов), пентозы (5 атомов), гексозы (6 атомов) и гептозы (7 атомов). Самыми распространенными моносахаридами являются пентозы и гексозы. Моносахариды хорошо растворимы в воде, легко кристаллизуются, имеют сладкий вкус, и могут быть представлены в форме α— или β-изомеров.
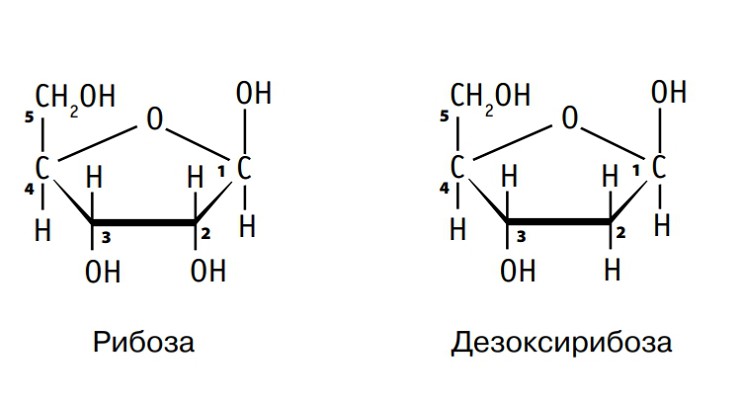
Моносахариды рибоза и дезоксирибоза, относящиеся к группе пентоз, входят в состав нуклеотидов РНК и ДНК — рибонуклеозидтрифосфатов и дезоксирибонуклеозидтрифосфатов, а также в состав др. веществ. Дезоксирибоза (С5Н10О4) отличается от рибозы (С5Н10О5) наличием при втором атоме углерода не гидроксильной группы, а атома водорода.
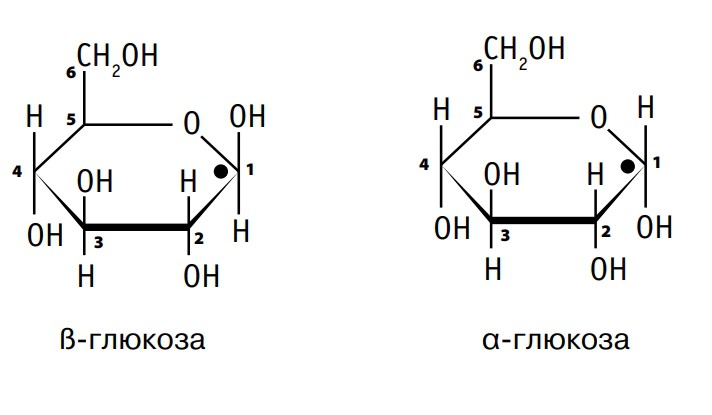
Одним из самых распространенных моносахаридов и важнейший источник энергии в клетке, является глюкоза, или виноградный сахар (С6Н12О6), которая относится к группе гексоз. Глюкоза может существовать в виде α-глюкозы или β-глюкозы. Отличие между этими пространственными изомерами заключается в том, что при первом атоме углерода у α-глюкозы гидроксильная группа расположена под плоскостью углеродного кольца, а у β-глюкозы — над плоскостью.
Энергия выделяется при окислении глюкозы в процессе дыхания. Кроме этого, значение глюкозы в том, что она является мономером многих полимерных углеводов — олигосахаридов и полисахаридов. Полимер — это высокомолекулярное соединение, состоящее из большого числа повторяющихся групп атомов, которые называют мономерами. Также глюкоза является необходимым компонентом крови. Ее содержание в крови — важный медицинский показатель.
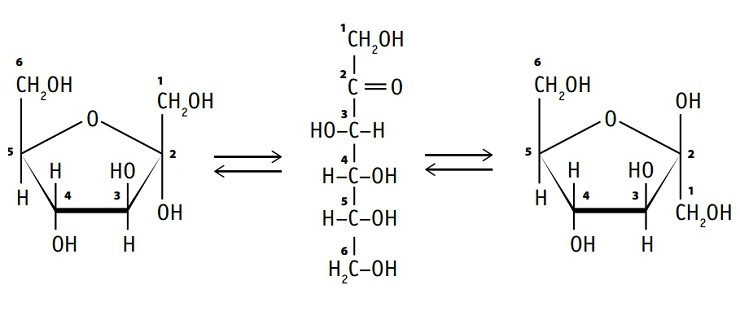
Другой представитель группы гексоз фруктоза или фруктовый сахар, (C6H12O6) более сладкая на вкус, чем глюкоза, в свободном виде содержится в меде и фруктах. Фруктоза — изомер глюкозы. Вспомните, что изомерами называют вещества, молекулы которых имеют одинаковые состав и молекулярную массу, но различаются строением или расположением атомов в пространстве.
Фруктоза может существовать в цепной или циклической формах.
Подобно глюкозе, фруктоза также является мономером многих олигосахаридов и полисахаридов.
Олигосахариды — углеводы, образованные несколькими (от двух до десяти) молекулами моносахаридов. В зависимости от числа остатков моносахаридов различают дисахариды, трисахариды и т. д. Наиболее распространены дисахариды. Олигосахариды хорошо растворимы в воде, кристаллизуются, их сладкий вкус снижается по мере увеличения числа остатков моносахаридов. Связь, образующаяся между двумя мономерами-моносахаридами называется гликозидной связью.
Сахароза, или тростниковый, или свекловичный сахар — дисахарид, состоящий из остатков глюкозы и фруктозы. Содержится в тканях растений. Является продуктом питания известным в быту под названием «сахар». В промышленности сахарозу получают из сахарного тростника стебли которого содержат 10–18% сахарозы или из сахарной свеклы, корнеплоды которой содержат до 20% сахарозы.
Мальтоза, или солодовый сахар — дисахарид, состоящий из двух остатков глюкозы, который присутствует в прорастающих семенах злаков.
Лактоза, или молочный сахар — дисахарид, состоящий из остатков глюкозы и галактозы. Присутствует в молоке всех млекопитающих (2 — 8%).
Полисахаридами называются углеводы, образованные более чем из десяти молекул моносахаридов (обычно моносахаридных остатков в молекулах полисахаридов несколько десятков и более). Полисахариды — не растворимы или плохо растворимы в воде, не образуют кристаллов и не имеют сладкого вкуса.
Крахмал (С6Н10О5)n — полисахарид, мономером которого является α-глюкоза. Полимерные цепочки крахмала содержат разветвленные и неразветвленные участки. Крахмал основной углевод нашей пищи. Крахмал является одним из продуктов фотосинтеза. Это основной резервный углевод растений накапливается в семенах, клубнях, корневищах, луковицах. Содержание крахмала в зернах риса достигает до 86%, пшеницы — до 75%, кукурузы — до 72%, в клубнях картофеля — до 25%. В том, что молекула крахмала состоит из глюкозы, можно убедиться путем простого опыта. Если долгое время (несколько минут) жевать какой-либо крахмалосодержащий продукт, например — кусочек хлеба или картофеля, то во рту появится сладкий вкус, обусловленный тем, что пищеварительный фермент амилаза, содержащийся в слюне, расщепил «несладкую» молекулу крахмала на составные части — «сладкие» молекулы глюкозы.
Гликоген (С6Н10О5)n — полисахарид, мономером которого также является α-глюкоза. Полимерные цепочки гликогена напоминают цепочки крахмала, но, в отличие от них, ветвятся гораздо сильнее. Гликоген является основным резервным углеводом грибов и животных, в том числе и человека. Он является источником глюкозы. Гликоген накапливается в печени, где его содержание достигает до 20% и в мышцах (до 4%).
Целлюлоза (С6Н10О5)n — полисахарид, мономером которого является β-глюкоза. Полимерные цепочки целлюлозы не ветвятся. Целлюлоза — основной структурный полисахарид клеточных стенок растений. Содержание целлюлозы в древесине достигает до 50%, а в волокнах семян хлопчатника (хлопок) — до 98%. Целлюлоза не расщепляется в организме человека, т.к. у нас отсутствует фермент целлюлаза, разрывающий связи между молекулами β-глюкозы.
Функции углеводов в живых организмах следующие:
Энергетическая (самая важная) — углеводы являются основным источником энергии всех клеточной жизнедеятельности. При расщеплении 1 г углеводов выделяется 17,6 кДж энергии.
Структурная — из целлюлозы состоит клеточная стенка растений, из углевода хитина — клеточная стенка грибов и покровы членистоногих.
Запасающая — резервным углеводом у животных и грибов является гликоген, у растений — крахмал.
Защитная — углеводы входят в состав слизи, предохраняющей бронхи и кишечник от механических повреждений.
БЕЛКИ ИЛИ ПРОТЕИНЫ — сложные высокомолекулярные вещества, состоящие из аминокислот (точнее — из остатков α-аминокислот). Обычно в качестве мономеров белков называют 20 видов α-аминокислот, хотя в клетках и тканях в целом их обнаружено свыше 170 видов. Белки обладают большой молекулярной массой: у яичного альбумина (то, что в быту называют «белком») она равна 36 000, у гемоглобина — 152 000, у мышечного белка миозина — 500 000. Сравните — молекулярная масса уксусной кислоты всего 60.
По содержанию в клетке белки стоят на втором месте после воды. Они составляют примерно 50% от сухого остатка клеточных веществ.
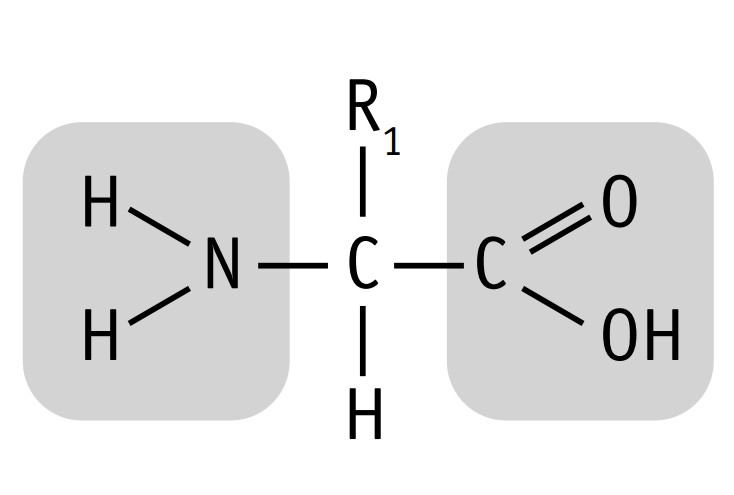
Все аминокислоты содержат карбоксильную группу (–СООН), аминогруппу (–NH2) и радикал или R-группу (остальная часть молекулы). Строение радикала различное у разных видов аминокислот. Аминокислоты являются амфотерными соединениями, т.е. в растворе они могут выступать как в роли кислот, так и оснований. В зависимости от количества аминогрупп и карбоксильных групп, входящих в состав аминокислот, различают: нейтральные аминокислоты, имеющие одну карбоксильную группу и одну аминогруппу; основные аминокислоты, имеющие более одной аминогруппы; кислые аминокислоты, имеющие более одной карбоксильной группы.
В зависимости от того, могут ли аминокислоты синтезироваться в организме человека или животных, их разделяют на заменимые аминокислоты, которые могут синтезироваться и незаменимые аминокислоты, синтезироваться которые не могут. Условием нормальной жизнедеятельности организма является поступление незаменимых аминокислот вместе с пищей.
ОБРАТИТЕ ВНИМАНИЕ! Растения синтезируют все виды аминокислот
В зависимости от аминокислотного состава, белки бывают: полноценными, содержащими в своих молекулах весь набор 20 основных аминокислот и неполноценными, в молекулах которых какие-то аминокислоты отсутствуют.
Белки, состоящие только из аминокислот, называют простыми. Если белки помимо аминокислот содержат еще и какой-то не аминокислотный компонент (металл, углевод, липид, нуклеиновую кислоту), то их называют сложными. Примерами сложных белков являются металлопротеины, гликопротеины, липопротеины, нуклеопротеины (название неаминокислотного компонента всегда ставится первым).
Белки относят к полипептидам. Пептидами называют вещества, молекулы которых построены из двух и более остатков аминокислот, соединенных в цепь пептидными (или амидными) связями —C(O)NH—. Для того, чтобы полипептид считался белком, его молекулярная масса должна быть выше 5000, в составе молекулы должно присутствовать более 50-90 аминокислотных остатков.
Клетке энергетически невыгодно (можно сказать — «неудобно») держать белки в развернутой форме, в виде полипептидной цепочки. К тому же выполнение белками ряда специфических функций зависит от пространственной конфигурации их молекул. Поэтому полипептидные цепи подвергаются пространственной организации — укладке с приобретением определенной трехмерной структуры.
Различают четыре уровня пространственной организации белков.
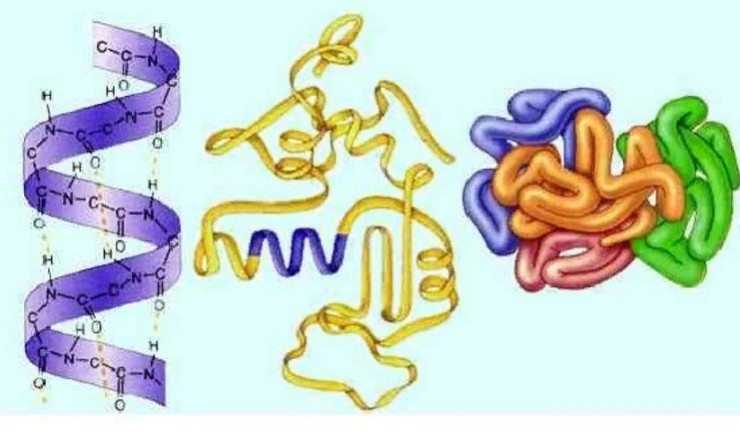
Первичная структура белка — полипептидная цепь.
ОБРАТИТЕ ВНИМАНИЕ! Первичная структура белковой молекулы определяет ее свойства и пространственную конфигурацию
Вторичная структура белка — упорядоченное свертывание полипептидной цепи в спираль, которая имеет вид растянутой пружины. Витки спирали укрепляются водородными связями, возникающими между карбоксильными группами СО— и аминогруппами NН-. (Вспомните о водородных связях из курса химии). Водородные связи слабее пептидных, но, многократно повторяясь, они придают спирали устойчивость и жесткость. На уровне вторичной структуры существуют такие белки, как, например, коллаген (сухожилия) или кератин (волосы, ногти).
Третичная структура белка представляет собой укладку полипептидных цепей в «клубки» — глобулы, возникающая в результате возникновения различных химических связей.
Связи эти могут быть водородными, ионными, дисульфидными (ковалентные связи между двумя атомами серы —S—S—, входящими в состав серосодержащей аминокислоты цистеина), но основную роль в образовании третичной структуры играют гидрофильно-гидрофобные взаимодействия между радикалами аминокислотных остатков.
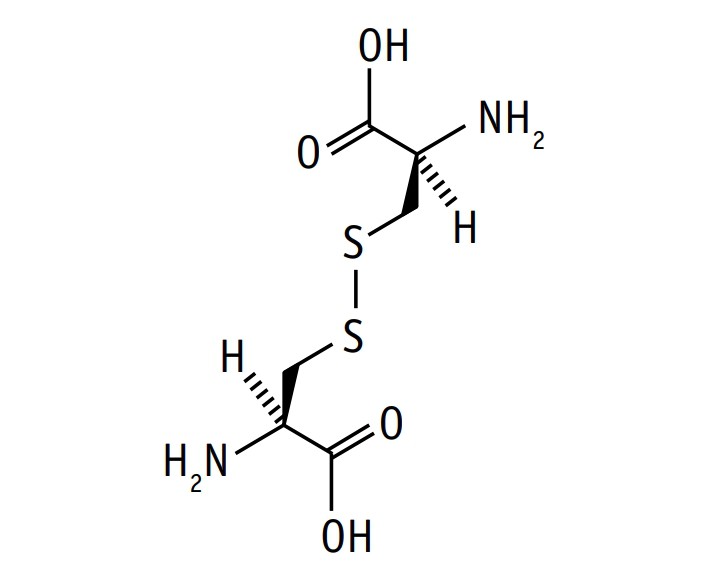
В водных растворах гидрофобные радикалы стремятся спрятаться от воды, группируясь внутри глобулы, в то время как гидрофильные радикалы в результате гидратации (взаимодействия с диполями воды) стремятся оказаться на поверхности молекулы (снова вспоминаем химию).
Молекула воды как диполь — система, состоящая из точечных и равных по абсолютной величине положительного и отрицательного электрических зарядов.
На уровне третичной структуры существуют ферменты, антитела, некоторые гормоны.
Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами, соединенными ионными, гидрофильно-гидрофобным и электростатическим взаимодействиями. Также между глобулами могут возникать дисульфидные связи.
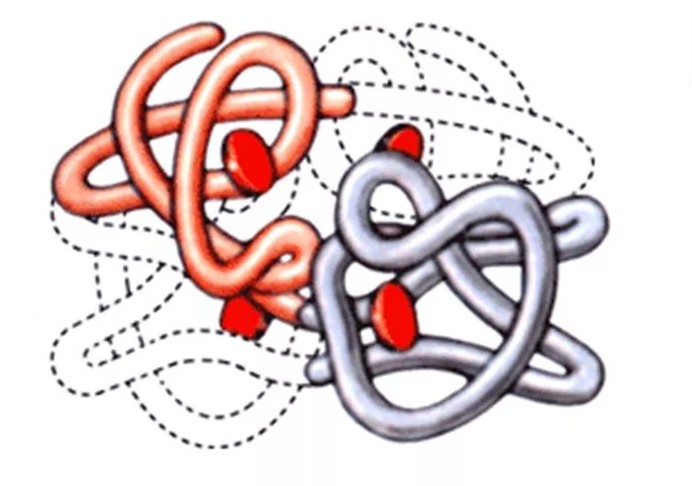
Наиболее известным белком, имеющим четвертичную структуру, является белок крови гемоглобин, молекула которого образована двумя α-субъединицами (141 аминокислотный остаток) и двумя β-субъединицами (146 аминокислотных остатков). С каждой субъединицей связана содержащая железо молекула гема.
Процесс утраты трехмерной конформации, присущей данной молекуле белка, называют денатурацией. Причиной денатурации является разрыв связей, стабилизирующих структуру белка. Сначала разрываются наиболее слабые связи, а при усилении дестабилизирующего фактора (например — нагревание) — более сильные. Следовательно, сначала утрачивается четвертичная, затем третичная, а затем вторичная структуры. Изменение пространственной конфигурации приводит к изменению свойств белка и делает невозможным выполнение присущих ему биологических функций. Если денатурация не сопровождается разрушением первичной структуры, то она может быть обратимой — не всегда, но в ряде случаев может произойти самовосстановление изначальной структуры. Процесс восстановления структуры белка после денатурации называется ренатурацией. Пример — рецепторные белки клеточных мембран в ходе выполнения своих функций (прием сигналов из внешней среды и передача команд в клетку) изменяют структуру. Если восстановление изначальной структуры белка невозможно, то денатурация называется необратимой. При варке куриного яйца в кипящей воде происходит необратимая денатурация белков, в результате чего они из жидкого состояния переходят в твердое.
Белки участвуют во всех процессах жизнедеятельности клетки.
Функции белков:
Строительная — белки участвуют в образовании клеточных и внеклеточных структур: входят в состав клеточных мембран (липопротеины, гликопротеины), сухожилий (коллаген), волос (кератин) и т.д.
Транспортная — например, гемоглобин присоединяет кислород и транспортирует его от легких ко всем тканям и органам, а от них в легкие переносит углекислый газ; в состав клеточных мембран входят белки, обеспечивающие избирательный перенос веществ и ионов (белковые каналы).
Каталитическая — белки, называемые ферментами, катализируют (ускоряют) происходящие в клетках биохимические реакции.
Двигательная — сократительные белки актин и миозин обеспечивают сокращение мышц у многоклеточных животных.
Регуляторная — гормоны белковой природы принимают участие в регуляции процессов обмена веществ. Например — инсулин регулирует содержание глюкозы в крови и углеводный обмен в целом.
Защитная — в ответ на проникновение в организм чужеродных белков или микроорганизмов (антигенов), образуются особые белки (антитела), способные их связывать (обезвреживать). Кроме того, фибрин, образующийся из белка фибриногена, способствует прекращению кровотечений.
Сигнальная — в поверхностную мембрану клетки встроены молекулы белков (рецепторы), способных изменять свою третичную структуру в ответ на действие факторов внешней среды.
Запасающая — чаще всего белки служат в качестве запаса питательных веществ в структурах, связанных с размножением (в семенах многих растений, в яйцах животных). Кроме этого, белки способны связываться с некоторыми веществами, удерживая их в организме. Например, при распаде гемоглобина железо не выводится, а сохраняется, образуя комплекс с белком ферритином.
Энергетическая — при распаде 1 г белка до конечных продуктов выделяется 17,6 кДж. Сначала белки распадаются до аминокислот, а затем до конечных продуктов — воды, углекислого газа и аммиака.
ОБРАТИТЕ ВНИМАНИЕ! В качестве источника энергии белки в организмах животных используются только после того, как будут израсходованы другие источники — углеводы и жиры
Ферменты или энзимы — это белки, являющиеся катализаторами биохимических реакций, которые при их участии протекают с огромной скоростью. Скорость ферментативных реакций отличается от скорости реакций, идущих с участием неорганических катализаторов примерно так же, как скорость сверхзвукового самолета отличается от скорости пешехода.
Вещество, на которое оказывает свое действие фермент, называют субстратом.
Ферменты представляют собой глобулярные белки, которые, как и все белки, подразделяются на простые и сложные. Простые ферменты являются простыми белками — состоят только из аминокислот. Сложные ферменты являются сложными белками — в их состав помимо белковой части входит группа небелковой природы, называемая кофактором. Часто в качестве кофакторов выступают витамины.
Для реакций ферментативного катализа характерны:
- высокая эффективность;
- строгая избирательность и направленность действия;
- точная регуляция;
- субстратная специфичность (способность фермента катализировать превращения только одного определенного субстрата или же группы сходных по строению субстратов).
По типу катализируемых химических превращений ферменты разделены на шесть классов: Оксиредуктазы, которые переносят атомы от одного вещества к другому. Пример — дегидрогеназа.
Трансферазы, которые переносят группы (метильную группу, аминогруппу и др.) от одного вещества к другому. Пример — трансаминаза.
Гидролазы, ускоряющие реакции гидролиза, при которых из субстрата образуются два продукта. Пример — амилаза, липаза.
Лиазы, обеспечивающие негидролитическое присоединение к субстрату или отщепление от него группы атомов. Пример — декарбоксилаза.
Изомеразы, участвующие в создании изомеров (внутримолекулярной перестройке атомов и групп). Пример — изомера-за.
Лигазы, катализирующие соединение двух молекул. Пример — синтетаза.
ЛИПИДЫ — это группа органических соединений, включающая жиры и жироподобные вещества.
Липиды разделяют на простые и сложные.
Простые липиды в большинстве своем представлены триглицеридами — сложными эфирами высших жирных кислот и трехатомного спирта глицерина Жирные кислоты имеют одинаковую для всех кислот группировку — карбоксильную группу (–СООН) и радикал, которым они отличаются друг от друга. Радикал представляет собой цепочку из различного количества (от 14 до 22) углеводородных группировок –СН2–. Если радикал жирной кислоты содержит одну или несколько двойных связей (–СН=СН–), такую жирную кислоту называют ненасыщенной, а если жирная кислота не имеет двойных связей, ее называют насыщенной. При образовании триглицерида каждая из трех гидроксильных групп глицерина вступает в реакцию конденсации с жирной кислотой с образованием трех сложноэфирных связей.
Если в триглицеридах преобладают насыщенные жирные кислоты, то их называют жирами. Жиры характерны для животных клеток. Если в триглицеридах преобладают ненасыщенные жирные кислоты, то их называют маслами. Масла характерны для растительных клеток. Одним из выраженных отличий между маслами и жирами является их разное агрегатное состояние при нормальных условиях (температуре в 20°С). Жиры твердые, а масла жидкие.
Плотность триглицеридов ниже плотности воды, поэтому в воде они всплывают.
К простым липидам также относят воски — сложные эфиры высших жирных кислот и высокомолекулярных спиртов. Воски устойчивы (обладают малой химической активностью), нерастворимы в воде, но хорошо растворимы в органических растворителях — бензине, хлороформе, эфире. Воски делятся на животные и растительные.
Животные воски:
- пчелиный воск, выделяемый специальными железами медоносных пчел, из которого пчелы строят соты;
- шерстяной воск или ланолин, предохраняющий шерсть (и кожу) животных от как от посторонней влаги, так и от высыхания;
- спермацет, содержащийся в организме кашалотов.
Растительные воски покрывают тонким слоем листья, стебли, плоды и защищают их от размачивания водой, высыхания и вредных микроорганизмов. Также воски в качестве резервных липидов могут входить в состав семян (например у симмондсии китайской, более известной под названием «жожоба»).
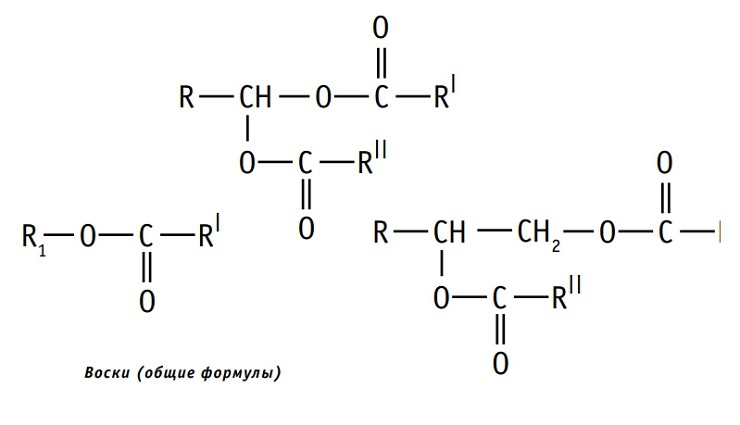
К сложным липидам относят фосфолипиды, гликолипиды, липопротеины и др. группы веществ. С многообразием липидов можно ознакомиться по схеме.
Фосфолипиды представляют собой триглицериды, у которых один остаток жирной кислоты замещен на остаток фосфорной кислоты. Как вы уже знаете, фосфолипиды входят в состав клеточных мембран.
Фосфолипиды подразделяются на глицерофосфолипиды и сфинголипиды. Глицерофосфолипиды являются производными фосфатидной кислоты: в их состав входят глицерин, жирные кислоты, фосфорная кислота и обычно азотсодержащие соединения.
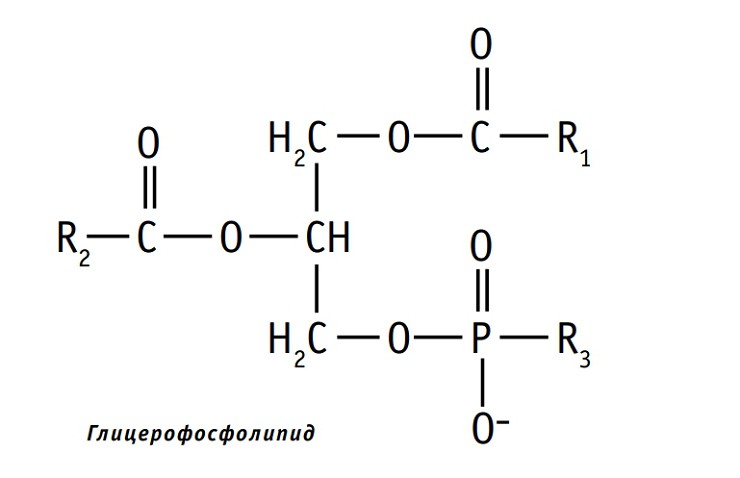
Характерным для всех глицерофосфолипидов является то, что одна часть их молекулы (радикалы R1 и R2) имеет резко выраженную гидрофобность, тогда как другая часть гидрофильна благодаря отрицательному заряду остатка фосфорной кислоты и положительному заряду радикала R3. Вспомните, что мы обсуждали это в прошлом разделе, когда говорили о строении клеточной мембраны.
Сфинголипиды, представляющие собой производные алифатических аминоспиртов, играют важную роль в передаче клеточного сигнала и в клеточном распознавании (способности организма отличать свои клетки от чужеродных). Сфинголипиды содержатся практически во всех клетках, но особенно богата ими нервная ткань.
Липопротеины представляют собой комплексные вещества, образующиеся в результате соединения липидов и белков. Липопротеины подразделяют на свободные, или растворимые в воде (липопротеины плазмы крови, молока и др.), и структурные или нерастворимые (липопротеины клеточных мембран, миелиновой оболочки нервных волокон, хлоропластов растений).
Липоиды — это различные жироподобные вещества, к которым относятся каротиноиды (фотосинтетические пигменты), стероидные гормоны (половые гормоны, минералокортикоиды, глюкокортикоиды), гиббереллины (ростовые вещества растений), жирорастворимые витамины (А, D, Е, К), холестерин, камфора и т.д.
Функции липидов:
Энергетическая — это основная функция триглицеридов. При расщеплении 1 г липидов выделяется 38,9 кДж энергии.
Структурная — фосфолипиды, гликолипиды и липопротеины принимают участие в образовании клеточных мембран.
Запасающая — жиры и масла являются резервным пищевым веществом у животных и растений. Особенно важны эти запасы для животных, впадающих в холодное время года в спячку (бурый медведь) или совершающих длительные переходы через местность, в которой нет источников пищи (верблюд).
Защитная — прослойки жировой ткани и жировые капсулы обеспечивают защиту внутренних органов. Слои воска используются в качестве защитного водоотталкивающего покрытия у растений и животных.
Теплоизоляционная — подкожная жировая клетчатка препятствует отдаче тепла в окружающее пространство. Это очень важно для всех водных млекопитающих (температура воды ниже температуры воздуха) и для млекопитающих, обитающих в холодном климате.
Регуляторная — например, липиды гиббереллины, относящиеся к растительным гормонам, регулируют рост растений, половой гормон тестостерон отвечает за развитие мужских вторичных половых признаков, а половой гормон эстроген отвечает за развитие женских вторичных половых признаков и осуществляет регуляцию менструального цикла. Минералокортикоиды (альдостерон и др.) регулируют водно-со-левой обмен, а глюкокортикоиды (кортизол и др.) принимают участие в регуляции углеводного и белкового обменов.
Служат источником метаболической воды — при окислении 1 кг жира выделяется 1,1 кг воды. Это свойство очень важно для обитателей пустынь.
Каталитическая — жирорастворимые витамины A, D, E, K являются кофакторами различных ферментов.
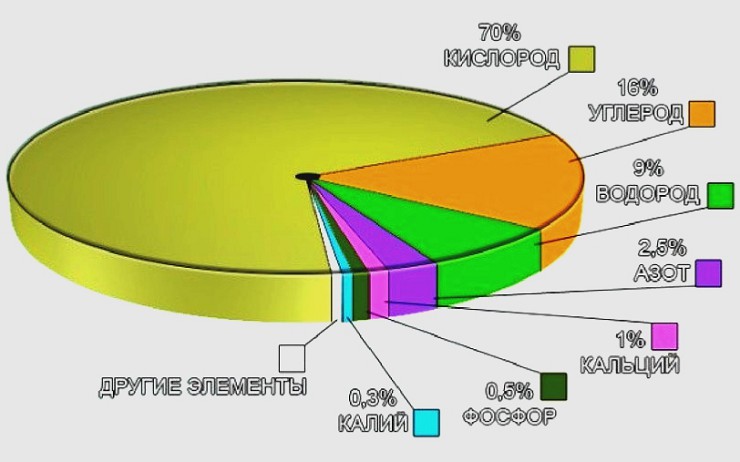
С перечнем и функциями основных ХИМИЧЕСКИХ ЭЛЕМЕНТОВ, содержащихся в клетке, вы можете ознакомиться по таблице. Заучивать наизусть ее не надо, важно иметь общее представление.
НУКЛЕИНОВЫЕ КИСЛОТЫ — это природные высокомолекулярные соединения, осуществляющие хранение, передачу и реализацию наследственной информации. Нуклеиновые кислоты представляют собой фосфорсодержащие биополимеры, мономерами которых служат нуклеотиды. Нуклеотиды — это соединения, в состав которых входят моносахарид (дезоксирибоза или рибоза, относящиеся к пентозам), фосфатная группа (остаток молекулы фосфорной кислоты) и азотсодержащее (азотистое) основание — аденин (у ДНК и РНК), гуанин (у ДНК и РНК), цитозин (у ДНК и РНК), тимин (только у ДНК), урацил (только у РНК).
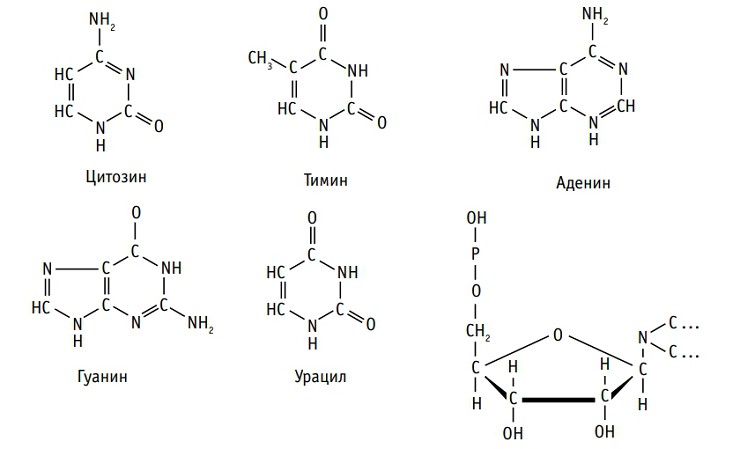
Название нуклеотида является производным от названия соответствующего основания — адениловый, гуаниловый и т.п.
В зависимости от того, какой моносахарид (рибоза или дезоксирибоза) входит в состав нуклеотида, различают два класса нуклеиновых кислот: рибонуклеиновые кислоты (РНК) и дезоксирибонуклеиновые кислоты (ДНК).
ОБРАТИТЕ ВНИМАНИЕ! У эукариот ДНК линейная и находится в ядре, а у прокариот ДНК кольцевая и находится в особой области клетки — нуклеоиде, который не отделен мембраной от остальной цитоплазмы
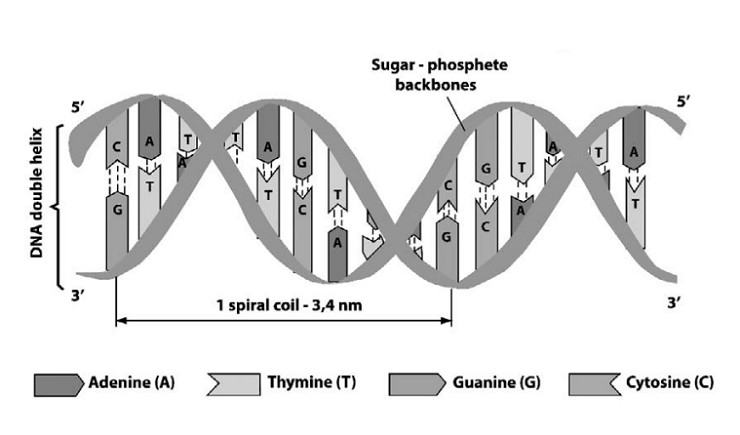
Молекула ДНК образована двумя полинуклеотидными цепями, спирально закрученными друг около друга и вместе вокруг воображаемой оси, т.е. она представляет собой двойную спираль. Исключение составляют некоторые ДНК-содержащие вирусы, которые имеют ДНК в виде одинарной цепочки.
Диаметр двойной спирали ДНК — 2 нм, расстояние между соседними нуклеотидами — 0,34 нм, на один оборот спирали приходится 10 пар нуклеотидов. Длина молекулы может достигать нескольких сантиметров и иметь молекулярный вес, исчисляемый десятками и сотнями миллионов единиц. Суммарная длина ДНК ядра одной клетки человека составляет около 2 метров.
Расположение нуклеотидов в двух парных цепях молекулы ДНК строго определенное: против аденина одной цепи в другой цепи всегда располагается тимин, а против гуанина — всегда цитозин. Между аденином и тимином возникают две водородные связи, между гуанином и цитозином — три водородные связи. Закономерность, согласно которой нуклеотиды разных цепей ДНК строго упорядоченно располагаются (аденин — тимин, гуанин — цитозин) и избира-тельно соединяются друг с другом, называется принципом комплементарности.
Из принципа комплементарности следует, что последовательность нуклеотидов одной цепи определяет последовательность нуклеотидов другой.
Функция ДНК — хранение и передача наследственной информации.
Давайте посмотрим на структурную формулу нуклеотида. Атомы углерода нумеруются в пентозе по часовой стрелке.
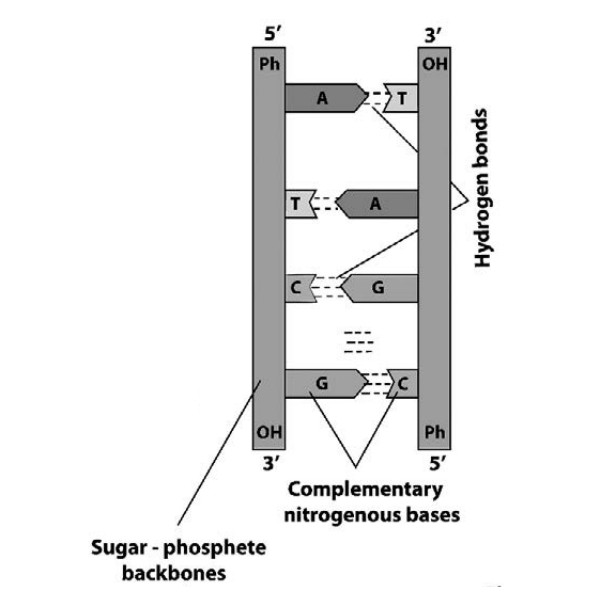
Можно сказать, что у нуклеотида два конца — 5’ и 3’ по номерам атомов углерода. Каждый из нуклеотидов в цепи связывается с последующим нуклеотидом посредством фосфорного остатка. При этом фосфорный остаток, связанный с третьим атомом углерода дезоксирибозы (3’-конец), соединяется с пятым атомом углерода дезоксирибозы второго нуклеотида (5’-конец). Только так и никак иначе.
Соответственно у каждой цепи нуклеотидов в молекуле ДНК есть 5’-конец и 3’-конец.
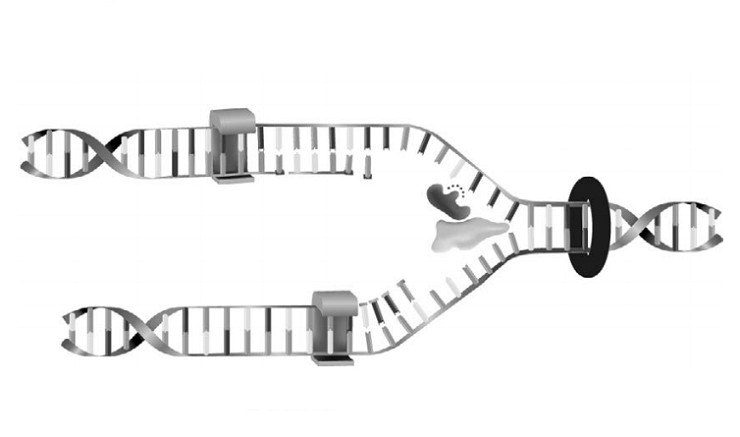
Две цепи, участвующие в построении молекулы ДНК, всегда разнонаправлены (антипараллельны) то есть имеют встречное расположение и 3’-конец одной цепи соответствует 5’-концу другой цепи. Этот принцип имеет большое значение при репликации ДНК, так как ферменты (ДНК-полимеразы) могут передвигаться вдоль матричных цепей только от 5’-конца к 3’-концу.
Репликация — это главное свойство молекулы ДНК, представляющее собой процесс самоудвоения. Репликация относится к категории реакций матричного синтеза, когда синтез новой цепи происходит по матрице — старой цепи, и проходит с участием ряда ферментов.
Ферменты, участвующие в репликации:
- хеликазы («расплетают» цепи ДНК);
- дестабилизирующие белки (связывают одноцепочечные участки ДНК, не давая им соединиться друг с другом);
- ДНК-топоизомеразы (разрезают ДНК); — ДНК-полимеразы (подбирают дезоксирибонуклеозидтрифосфаты и комплементарно присоединяют их к матричной цепи ДНК);
- ДНК-праймазы (по сути это РНК-синтетаза синтезирует короткий фрагмент РНК, называемый праймером, который «запускает» или «включает» ДНК-полимеразу на отстающей цепи);
- ДНК-лигазы (сшивают фрагменты ДНК).
ДНК-полимераза может присоединять нуклеотид только к 3’-углероду дезоксирибозы предыдущего нуклеотида, поэтому данный фермент способен передвигаться по матричной ДНК только в одном направлении: от 3’-конца к 5’-концу этой матричной ДНК.
Полинуклеотидных цепей две, они антипараллельны, а ДНК-полимераза одна и способна двигаться только в одном направлении. Как же происходит синтез?
На цепи 3’–5’ синтез дочерней полинуклеотидной цепи идет последовательно без перерывов и эта дочерняя цепь назы-вается лидирующей. На цепи 5’–3’ синтез производится с участием «запускающего» фермента ДНК-праймазы и про-ходит прерывисто, фрагментарно. Фрагменты, которые называются фрагментами Оказаки, сшиваются в одну цепь ДНК-лигазами. Вторая дочерняя цепь называется запаздывающей отстающей, потому что ее синтез отстает от синтеза лидирующей цепи.
Строительным материалом и источником энергии для репликации являются дезоксирибонуклеозидтрифосфаты (АТФ, ТТФ, ГТФ, ЦТФ), содержащие три остатка фосфорной кислоты. При включении дезоксирибонуклеозидтрифосфатов в полинуклеотидную цепь два концевых остатка фосфорной кислоты отщепляются. Освободившаяся при этом энергия используется для образования фосфодиэфирной связи между нуклеотидами.
Скорость синтеза ДНК у эукариот идет со скоростью пример-но 100 нуклеотидов в секунду, а у прокариот она на порядок выше -1000 нуклеотидов в секунду! Репликация начинается одновременно в нескольких участках молекулы ДНК. Фрагмент ДНК от одной точки начала репликации до другой образует единицу репликации, называемый репликоном.
Благодаря способности репликации ДНК осуществляется передача наследственной информации от материнской клетки дочерним.
Скажите, а когда происходит репликация ДНК? Перед делением клетки, в периоде синтеза интерфазы митоза!
Участок молекулы ДНК и некоторых РНК, содержащий информацию о биосинтезе одной полипептидной цепи с определенной аминокислотной последовательностью, т.е. содержащий информацию об одном признаке организма, называют геном.
Систему записи наследственной информации в виде последовательности нуклеотидов в молекулах нуклеиновых кислот, называют генетическим кодом.
Дискретная единица генетического кода, состоящая из трех соседних последовательных нуклеотидов (триплет), называется кодоном. Кодон кодирует включение в полипептидную цепь одной аминокислоты. Последовательность кодонов в гене определяет последовательность аминокислот в полипептидной цепи белка, кодируемого этим геном. Всего возможно 64 сочетания нуклеотидов в триплетах. 61 из являются кодонами, определяющими 20 аминокислот, а 3 так называемыми терминирующими или стоп-кодонами, которые определяют окончание синтеза полипептидной цепи.
РНК — полимер, мономерами которой являются рибонуклеотиды, т.е. нуклеотиды, содержащие рибозу. В отличие от ДНК, РНК образована не одной полинуклеотидной цепочкой. Исключение составляют некоторые РНК-содержащие вирусы, которые имеют двухцепочечную РНК. Цепи РНК значительно короче цепей ДНК.
Вы уже знаете, что РНК бывает четырех видов: информационная или матричная РНК (иРНК или мРНК), транспортная РНК (тРНК), рибосомная РНК (рРНК) и ферментативные РНК (рибозимы).
Все виды РНК принимают участие в процессах синтеза белков — трансляции.
Информация о строении всех видов РНК хранится в ДНК.
Процесс синтеза РНК на матрице ДНК называется транскрипцией.
Транспортные РНК, на долю которых приходится около 10% от общего содержания РНК в клетке, не только транспортируют аминокислоты к месту синтеза белка, но и выполняют посредническую функцию в синтезе. В клетке встречается около 40 видов тРНК, но у всех тРНК имеется несколько внутримолекулярных комплементарных участков (участков, образующих связи между собой), из-за которых тРНК приобретают пространственную структуру, напоминающую по форме лист клевера.
У любой тРНК есть петля для контакта с рибосомой (1), антикодоновая петля (2), петля для контакта с ферментом (3), акцепторный стебель (4), антикодон (5). Аминокислота присоединяется к 3’-концу акцепторного стебля. Антикодон это три нуклеотида. Конкретная тРНК может транспортировать строго определенную аминокислоту, соответствующую ее антикодону.
Рибосомные РНК составляют 80–85% от общего содержания РНК в клетке. В комплексе с рибосомными белками они образуют рибосомы — органоиды, осуществляющие синтез белка. В эукариотических клетках синтез рРНК происходит в ядрышках. рРНК обеспечивает функционирование рибосом, будучи их структурным компонентом, а также обеспечивает взаимодействие рибосомы и тРНК.
Информационные РНК разнообразны по содержанию нуклеотидов. На их долю приходится до 5% от общего содержания РНК в клетке. иРНК переносят генетическую информацию от ДНК к рибосомам, служат матрицами для синтеза белковых молекул и определяют аминокислотную последовательность структуры белковой молекулы.
Рибозим (производное от «рибонуклеиновая кислота» и «энзим»), также называемый ферментативной РНК или каталитической РНК — это РНК, обладающая каталитическим действием. Рибозимы катализируют процессы расщепления молекул РНК и образования пептидных связей в белках. Рибозимы довольно широко применяются в медицине для борьбы с вирусными инфекциями. Это применение основано на способности рибозимов связываться с определенными участками вирусной иРНК и разрезать ее на куски. В результате исчезновения целостной полноразмерной иРНК, прекращается синтез соответствующего ей белка, т.е. прекращается размножение вируса.
Процессы синтеза являются важнейшей частью метаболизма в живых клетках.
Фотосинтез — это процесс образования органических веществ из неорганических с помощью солнечной энергии, свойственный растениям и некоторым бактериям, клетки которых содержат пигмент хлорофилл. Солнечная энергия, поглощенная хлорофиллсодержащей клеткой, преобразуется в химическую энергию органических соединений, т.е. запасается в их молекулах.
В основе фотосинтеза лежит окислительно-восстановительный процесс с образованием углевода и выделением молекулярного кислорода (O2) в случае окисления воды. Фотосинтезирующие бактерии зачастую используют для окисления не воду, а другие вещества, и кислород при этом не образуется.
Сущность фотосинтеза с использованием воды можно выразить следующей формулой:
6СО2 + 6Н2О + Qсвета → С6Н12О6 + 6О2
У высших растений органом фотосинтеза является лист, органоидами фотосинтеза — хлоропласты (пластиды).
Давайте немного вспомним ботанику.
Одним из главных компонентов процесса фотосинтеза является зеленый пигмент хлорофилл. Молекула хлорофилла способна запасать энергию света в виде энергии возбужденных электронов и преобразовывать ее в энергию химических связей. Хлоропласты имеют зеленый цвет, благодаря присутствию хлорофилла. В них также присутствуют вспомогательные пигменты фотосинтеза оранжевого цвета — каротиноиды.
Хлоропласты это овальные линзовидные тельца размером (5-10) х (2-4) мкм. В одной клетке листа может находиться 15-20 и более хлоропластов, а у некоторых водорослей только 1-2 гигантских хлоропласта (хроматофора).
Хлоропласты ограничены двумя мембранами — наружной и внутренней. Наружная мембрана отграничивает жидкую внутреннюю гомогенную среду хлоропласта строму (матрикс), в которой содержатся белки, липиды, ДНК, РНК, рибосомы, ферменты, участвующие в фиксации углекислого газа и запасные вещества (липиды, крахмальные и белковые зерна). Внутренняя мембрана хлоропласта образует впячивания внутрь стромы, которые имеют форму уплощенных мешочков. Их называют тилакоидами. Тилакоиды состоят из мембраны, окружающей просвет тилакоида.
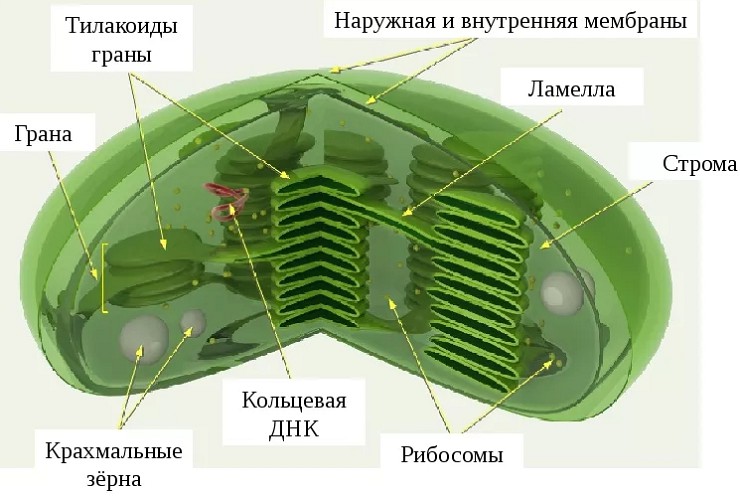
Тилакоиды могут располагаться один над другим, образуя граны, которые соединены между собой тилакоидами стромы, называемыми ламеллами. В мембранах тилакоидов находятся светочувствительные пигменты, а также переносчики электронов и протонов, участвующие в поглощении и преобразовании энергии света.
Фотосинтез — сложный многоступенчатый процесс; реакции фотосинтеза подразделяют на две группы: реакции световой фазы и реакции темновой фазы.
Световая фаза называется так, поскольку происходит только в присутствии света.
Под действием энергии света электроны хлорофилла возбуждаются, с помощью белков-переносчиков электронов покидают молекулу и попадают на внешнюю сторону мембраны тилакоида, придавая ей отрицательный заряд. Молекулы хлорофилла восполняют потерю, т.е. восстанавливаются, отбирая электроны у воды, находящейся внутри тилакоида, что приводит к фотолизу воды, распаду с использованием энергии света:
Н2О + Qсвета → Н+ + ОН—
Ионы гидроксила отдают свои электроны, превращаясь в реакционноспособные радикалы •ОН:
ОН— → •ОН + е—
Радикалы •ОН объединяются, образуя воду и свободный кислород:
4НО• → 2Н2О + О2
Кислород удаляется во внешнюю среду, а протоны Н+ накапливаются внутри тилакоида в «протонном резервуаре». В результате мембрана тилакоида с одной стороны заряжается положительно за счет протонов Н+, а с другой — отрицательно за счет электронов.
В мембране тилакоидов присутствует фермент, называемый АТФ-синтетазой (АТФ-синтазой), молекула которого состоит из двух частей: встроенного в мембрану протонного канала и активной каталитической субъединицы, выступающей в матрикс. Когда разность потенциалов между наружной и внутренней сторонами мембраны тилакоида достигает 200 мВ, протоны проталкиваются через каналы АТФ-синтетазы и происходит фосфорилирование находящегося в матриксе АДФ до АТФ. Атомарный водород расходуется на восстановление специфического переносчика протонов и электронов НАДФ (никотин-амидадениндинуклеотидфосфат) до НАДФ·Н2:
2Н+ + 2е— + НАДФ → НАДФ·Н2
Восстановление НАДФ+ идет с поглощением энергии.
Итак, в световую фазу в хлоропластах происходит фотолиз воды, который сопровождается тремя процессами — синтезом АТФ, образованием НАДФ·Н2 и образованием кислорода. Кислород уходит в атмосферу. АТФ и НАДФ·Н2 принимают участие в процессах темновой фазы фотосинтеза.
ОБРАТИТЕ ВНИМАНИЕ! Темновая фаза, протекающая в матриксе хлоропласта, названа так, поскольку для ее реакций не нужна энергия света. Но это не ночная фаза, которая происходит только ночью. Реакции темновой фазы идут и днем, и ночью
Реакции темновой фазы представляют собой цепочку последовательных преобразований поступающего из воздуха углекислого газа, с образованием глюкозы и других органических веществ. В этих реакциях используются энергии АТФ и НАДФ·Н2, образованных в световую фазу.
Благодаря фотосинтезу из атмосферы поглощается углекислый газ, а в нее выделяется кислород. Кроме того, фотосинтез является основным источником образования органических веществ на нашей планете.
Интересные цифры: при фотосинтезе растения используют всего 1% падающей на них солнечной энергии; продуктивность фотосинтеза составляет примерно 1 грамм органического вещества на 1 кв. метр поверхности зеленых листьев в час.
Фотосинтезирующими организмами являются многие группы бактерий, в частности цианобактерии. У бактерий нет пластид, поэтому фотосинтез происходит в цитоплазме и во внутриклеточных мембранах — мезосомах, бактериальных аналогов тилакоидов. На мезосомах находятся фотосинтезирующие пигменты (бактериохлорофиллы), здесь осуществляется световая фаза фотосинтеза, а темновая фаза проходит в цитоплазме клетки.
При хемосинтезе, который наблюдается у ряда бактерий, усвоение углекислого газа и преобразование его в органические вещества происходит за счет окисления неорганических соединений — сероводорода, серы, аммиака, водорода, азотистой кислоты, оксидных соединений двухвалентного железа и др.
Биологическим синтезом (биосинтезом) называют происходящий в живых организмах процесс образования органических веществ из более простых соединений. Биосинтез — основа жизнедеятельности, ведь посредством его образуются вещества и структуры, из которых строится организм, производится постоянное обновление клеток, осуществляется обмен веществ.
Биосинтез осуществляется с помощью биологических катализаторов — ферментов.
ОБРАТИТЕ ВНИМАНИЕ! Биосинтез осуществляется с потреблением энергии. Всегда! В результате процессов биосинтеза выделения энергии происходить не может! Энергию организмы получают разложением сложных веществ на более простые
Биосинтез, протекающий с использованием солнечной энергии, называют автотрофным. Автотрофный биосинтез может быть фототрофным (фотосинтез в клетках зеленых растений и некоторых бактерий) и хемотрофным (хемосинтез). Автотрофный биосинтез является определяющим процессом жизни на Земле, так как в ходе его образуются первичные сложные органические вещества, аккумулирующие энергию в своих химических связях.
Гетеротрофный биосинтез осуществляющийся за счет энергии, получаемой из сложных органических соединений. Характерной особенностью гетеротрофного биосинтеза является сочетание энергетического и синтетического процессов — разложение органических веществ, поступивших в клетку, ведет к синтезу веществ, необходимых для жизнедеятельности клетки.
Основу биосинтеза составляет биосинтез белка, поскольку все живое на нашей планете представляет собой белковую форму жизни.
В биосинтезе белка участвуют различные молекулы РНК, рибосомы и мономерные молекулы — аминокислоты, из которых строится полимерная белковая молекула. Молекулы РНК — строители, рибосомы — стройплощадка, и молекулы аминокислот — кирпичи.
Что нужно для начала строительства в первую очередь?
План! Нужно знать, что и как строить.
План строения белка закодирован в молекуле ДНК, которая служит матрицей для синтеза информационной (матричной) РНК — иРНК (мРНК). Процесс синтеза белка разделяется на два этапа: этап создания иРНК и этап непосредственного синтеза молекулы белка по заключенной в молекуле иРНК информации. Первый этап получил название транскрипция (от латинского слова «транскрипцио», означающего «переписывание») поскольку создание иРНК, представляет собой переписывание информации с молекулы ДНК. Второй этап — этап создания молекул белка — называют трансляцией (от латинского слова «трансляцио», означающего «передача», «перенесение»).
Цепь иРНК синтезируется непосредственно на одной из двух цепей молекулы ДНК, выступающей в роли матрицы, с помощью особого фермента — РНК-полимеразы, передвигающегося вдоль цепи ДНК в направлении 5’ → 3’. Синтезируемая цепь иРНК точно копирует нуклеотидную последовательность ДНК-матрицы по принципу комплементарности, но обратите внимание на то, что тимину (Т) в ДНК соответствует урацил (У) в РНК.
Первичная РНК (преРНК) должна «созреть», чтобы стать иРНК готовой для синтеза белка. В ходе «созревания» мРНК подвергается сплайсингу (удаляются интроны, участки, которые не кодируют белки, а экзоны, участки, кодирующие белки, сшиваются и образуют единую молекулу) и ряду других процессов. «Зрелая» иРНК выходит из ядра в цитоплазму, соединяется с рибосомой и начинается второй этап — трансляция, синтез белка из аминокислот.
Мы рассмотрели синтез белка в эукариотной клетке. У прокариот этот процесс проходит иначе, но сущность его сводится к тому же — считыванию генетической информации и синтезу на ее основании белка.
Биосинтез белка — часть пластического обмена, совокупности реакций синтеза органических веществ в клетке с использованием энергии, полученной в результате энергетического обмена.
