Как ведут себя атомы в реакциях?
В целом атом нейтрален. Когда атом теряет или приобретает элек троны, он становится электрически заряженным и превращается в ион.
Магниты не только притягиваются друг к другу, но и отталкиваются
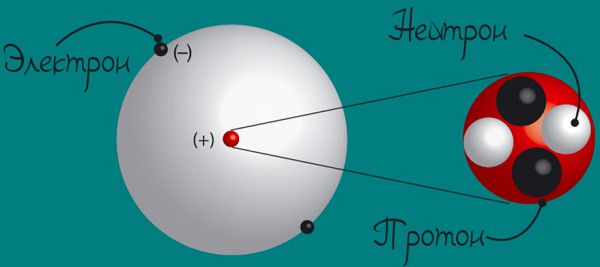
Ты уже знаешь, что магниты притягиваются друг к другу. Но если один из магнитов перевернуть, то они, наоборот, будут отталкиваться. Это происходит потому, что у каждого магнита есть два полюса: северный и южный. Одноименные полюсы отталкиваются, а разноименные — притягиваются. Ты можешь спросить: «А при чем здесь магниты? Какая связь между магнитами и атомами?» Оказывается, так же отталкиваются или притягиваются мельчайшие частицы, из которых состоит все, что нас окружает. В состав атома входят электроны - отрицательно заряженные частицы — и ядро, состоящее из положительно заряженных протонов и незаряженных нейтронов. Так как протоны и электроны имеют противоположные заряды, то они притягиваются друг к другу. Количество электронов всегда равно количеству протонов.
Опыт резерфорда
Сейчас мы с тобой проведем виртуальный опыт. Представь источник положительно заряженных частиц, или альфа-частиц, в виде небольшого шарика, находящегося в полностью герметичной коробке. Затем в одной из стенок коробки мы проделаем небольшую дырочку и перед отверстием поставим экран. Как только альфа-частицы вырываются из коробки и попадают на экран, они вызывают его свечение. А если между экраном и источником альфа-частиц поместить тонкую фольгу, то мы увидим следующее. Одни частицы как летели, так и продолжают долетать до экрана через фольгу, абсолютно ее не замечая. Другие — несколько отклоняются от траектории своего полета и меняют его направление, а третьи частицы, долетая до фольги, возвращаются назад, к источнику. В 1911 г. именно такой опыт провел английский физик Эрнест Резерфорд.
Выводы ученого
На основании этого опыта Резерфорд сделал вывод, что в центре атома находится положительно заряженное ядро, которое отталкивает альфа-частицы. Также ученый предложил ядерную модель строения атома. Согласно модели Резерфорда, почти вся масса атома сосредоточена в положительно заряженном ядре. Но так как большинство альфа-частиц пролетало сквозь фольгу без всяких отклонений, он предположил, что ядро занимает весьма незначительную часть объема атома. Положительное ядро окружено отрицательно заряженными электронами. Электронная оболочка занимает весь объем атома, но ее масса из-за легкости электронов несущественна.

Ионная и ковалентная связь
Атом считается более стабильным, если его внешняя орбита полностью заполнена электронами. В случае, если у атома есть свободные места на орбите, он будет вступать в химические реакции до тех пор, пока не заполнит все пустые места электронами.
Химики выяснили, что этот процесс может происходить тремя разными способами:
- Некоторые атомы отдают или принимают электроны и превращаются в ионы. Ионы могут быть как положительно, так и отрицательно заряженными. Ионы противоположного заряда притягиваются друг другу и образуют ионные соединения.
- Бывает так, что атомы делятся своими электронами с другими атомами. В таком случае внешняя оболочка всех атомов становится заполненной, и образуется молекула.
Такое распределение электронов между атомами называется ковалентной связью.
- Атомы металлов объединяются в огромные кристаллические решетки со строго определенным порядком. Причем именно разница в заряде заставляет атомы образовывать эти решетки.
ЗАПОМНИ! Передача электронов от атома к атому называется ионной связью.
