Дизайнерские дети
Фрэнсис Коллинз из Национального исследовательского института генома человека: «Богатые родители, решившие, что они хотят музыканта-виртуоза, будут разочарованы, когда их сын превратится в угрюмого подростка, который курит марихуану и не разговаривает с ними»
Дебби Эдвардс думала, что у нее никогда не будет детей. Ее племянник унаследовал генетическое заболевание адренолейкодистрофию, и анализ показал, что она тоже несет эту мутацию на одной из своих Х-хромосом. Поскольку ее вторая Х-хромосома несла работающую копию гена, миссис Эдвардс была абсолютно здорова. Но если бы она зачала сына, то у него с вероятностью 50 % наблюдалось бы прогрессирующее повреждение мозга, и он бы рано умер. Она приняла тяжелое решение не заводить семью.

Однако 15 июля 1990 года в больнице Хаммерсмит (Лондон) миссис Эдвардс родила здоровых двойняшек Натали и Даниэль. Она не поменяла своего мнения об опасности адренолейкодистрофии, просто наука нашла способ избежать этого заболевания. Развитие технологий тестирования эмбрионов дало миссис Эдвардс возможность забеременеть, и она была уверена, что у нее родятся здоровые дети.
Команда из больницы Хаммерсмита под руководством Алана Хэндисайда и Роберта Уинстона создала эмбрионы путем экстракорпорального оплодотворения (ЭКО) и вырастила их в лаборатории до стадии восьми клеток. Затем из каждого эмбриона удалили по одной клетке, и ученые исследовали их половые хромосомы, чтобы узнать, какие эмбрионы мужского пола, а какие — женского. Поскольку адренолейкодистрофия сцеплена с Х-хромосомой и встречается только у мальчиков, в матку миссис Эдвардс имплантировали только женские эмбрионы. Эта процедура называется преимплантационной генетической диагностикой (ПГД), и Натали и Даниэль стали первыми примерами того, что СМИ довольно вульгарно окрестили «дизайнерскими детьми».
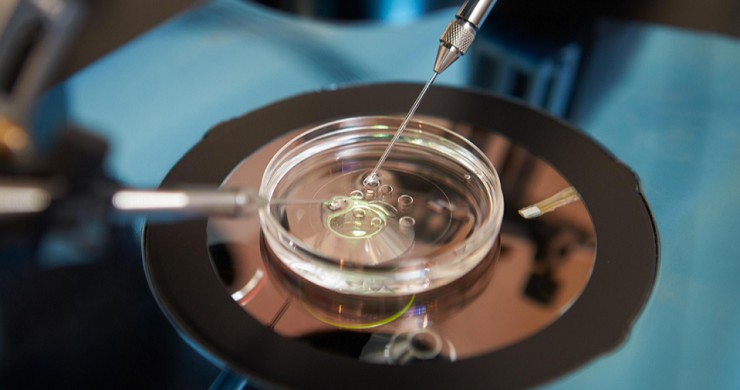

Революция ПГД
Рожденные путем ПГД дети на самом деле не были спроектированы. Их ДНК не изменяли, но термин «дизайнерские дети» закрепился, поскольку технология позволяет родителям делать что-то, что раньше было невозможным. Однако они не могут выбирать потенциальных детей на основе генетических качеств - так что процесс этот мало похож на пошив дизайнерского платья.
Технология позволила парам, знающим о том, что они могут передать тяжелое наследственное заболевание, иметь здоровое потомство. Сначала чувствительности ПГД хватало только на предупреждение Х-сцепленных заболеваний, например гемофилии или мышечной дистрофии Дюшена, но вскоре стало возможно проверять на наличие аутосомных болезней, включая муковисцидоз и болезнь Хантингтона. Так предупреждаются более 200 заболеваний, и благодаря ПГД в мире родилось несколько тысяч здоровых младенцев.
Однако метод вызывает этические споры. Люди, выступающие против разрушения зародышей, считают ПГД аморальным, поскольку эмбрионы с генетическими мутациями выкидывают или отдают на медицинские опыты. Особенно спорным является его применение по отношению к таким генам, как BRCA1. Мутации этого гена значительно увеличивают риск рака груди, но не всегда его вызывают, и унаследовавшие их женщины могут себя защитить, хотя и посредством уродующей профилактической операции. Критики считают тестирование эмбрионов формой евгеники, искоренением болезни за счет убийства ее носителя.
ПГД также стало спасением для детей, страдающих от таких заболеваний, как лейкемия и анемия, которым нужна пересадка донорского костного мозга. Если донора нет, родители могут попробовать завести еще одного ребенка и проверить эмбрионы на совпадение с уже живущим. В 2002 году американская девочка Молли Нэш, страдавшая анемией Фанкони, стала первым пациентом, вылеченным тканью такого «брата-спасителя». Она получила стволовые клетки из пуповины своего новорожденного брата Адама, чей тип ткани был определен в состоянии эмбриона.
Это применение ПГД также у многих вызывает сомнения. Процесс биопсии несет небольшой риск для эмбриона, и существует мнение, что не стоит подвергать зародыши этой процедуре. Британское Управление по оплодотворению и эмбриологии человека поначалу разрешило типирование тканей эмбрионов, но только если они еще и проверяются на заболевания. Впоследствии оно отменило это решение, когда была доказана безопасность процедуры.
«Мы все на скользкой дорожке. Нам надо лишь решить — лыжи или кошки?» Джон Харрис, профессор биоэтики Манчестерского университета
Скользкая дорожка?
Несогласие с практикой ПГД основывается еще на одном аргументе: если семьям, желающим избежать рождения больного младенца или заводящим ребенка-донора, столь легко этого добиться, то это вселяет тревогу. При таком подходе общество встает на скользкую дорожку, которая ведет прямиком к тестированию эмбрионов на гены, влияющие на интеллект, рост или внешность. Дети становятся продуктом — по крайней мере, для тех, кто может позволить себе эту технологию.
Но общество вполне может разрешить одно применение ПГД, а другое запретить. По социальным причинам в Великобритании запрещено использование ПГД для выбора пола ребенка или сознательной отбраковки инвалидов, но разрешено для предупреждения болезни.
Антиутопичный потенциал технологии также ограничен наукой. Во-первых, для ПГД всегда требуется ЭКО, которое ни к чему людям, способным зачать самостоятельно. Во-вторых, надо знать, что искать. Свойства, которые могут захотеть настойчивые родители, например, интеллект или атлетизм, управляются десятками генов, взаимодействующими друг с другом сложными путями, и условиями внешней среды. Невероятно сложно протестировать все эти гены и гарантировать желаемый исход.
Также существует проблема сырья. Эмбриологи, использующие ПГД, работают с тем, что дает природа, то есть с генами родителей. Можно попробовать заказать младенца с мозгами Стивена Хокинга и внешностью Кейт Мосс, но если мама и папа не обладают этими свойствами, ничего не выйдет.
ПГД является незаменимым инструментом предупреждения генетических заболеваний, передающихся от поколения к поколению и обрекающих целые семьи на несчастья и страдания. Но оно совершенно не подходит для массового производства детей на заказ.
Преимплантационное генетическое тестирование

Метод биопсии эмбрионов также применяется при лечении бесплодия — для проверки генетического качества эмбрионов и увеличения шансов успешной беременности. Если эмбрион несет слишком много или слишком мало хромосом, то, скорее всего, беременность закончится выкидышем, и тестирование позволяет отобрать для переноса в матку только нормальные эмбрионы.
В Великобритании лицензии на проведение такого преимплантационного генетического тестирования есть у восьми клиник. Им разрешено проводить процедуру для женщин с историей выкидышей или неудачного ЭКО, однако существуют сомнения в эффективности метода. В 2007 году голландское исследование показало, что технология способна даже уменьшать число удачных ЭКО — возможно, потому, что биопсия повреждает эмбрион. Защитники метода указывают на множество неточностей в этом исследовании и доказывают, что при правильном проведении он эффективен.
Искусственные хромосомы
ПГД позволяет только выбирать между эмбрионами, несущими генетические профили родителей, но истинные «дизайнерские дети» вполне реальны в будущем — благодаря сложной генетической инженерии. Один из возможных методов — создание синтетических хромосом, специально спроектированных для переноса полезных генов и вводимых в эмбрион на ранней стадии развития.
Данный подход не станет реальностью еще десятки лет, но у него есть два преимущества. Он не нарушит генетическую последовательность существующих хромосом, что снизит риск ошибки, вызывающей такие болезни, как рак. И биофизик Грегори Сток, защитник генетических улучшений, предположил, что такие хромосомы можно будет активировать уже после рождения ребенка, тогда, повзрослев, ребенок сам решит, хочет ли включить свои генетические модификации.
