Простые вещества
Ради открытия новых простых веществ - то есть состоящих из атомов одного химического элемента - химики пускаются во все тяжкие. Периодическая таблица элементов подсказывает нам, в каком примерно порядке происходили открытия, но это не просто список элементов. Закономерности Периодической таблицы описывают природу простых веществ, а также особенности их взаимодействия друг с другом.
Немецкий алхимик XVII века Хенниг Бранд (ок. 1630 — ок. 1710) был золотоискателем. Женившись, он бросил службу в армии и вложил приданое жены в поиски философского камня — мифического вещества или минерала, о котором алхимики грезили многие века. Легенда гласит, что философский камень способен трансмутировать обычные металлы вроде железа или свинца в золото. После смерти первой супруги Бранд нашел себе вторую и продолжил поиски в том же духе. Судя по всему, он решил, что философский камень можно синтезировать из телесных жидкостей, и приобрел ни много ни мало 1500 галлонов человеческой мочи, из которой вознамерился экстрагировать волшебное вещество. Наконец в 1669 году он сделал поразительное открытие, хоть и не философского камня. В ходе экспериментов, при кипячении и упаривании мочи, Бранд нечаянно стал первым человеком, получившим простое вещество с применением химических методов.

Бранд добыл вещество, содержащее фосфор, которое он назвал холодным огнем, потому что оно светилось в темноте. Но простым веществом фосфор признали только в 1770-х годах. К тому времени простые вещества открывали сплошь и рядом: всего за десятилетие химики выделили кислород, азот, хлор и марганец.
В 1869 году, через два века после открытия Бранда, русский химик Дмитрий Менделеев составил Периодическую таблицу, и фосфор занял в ней положенное ему место — между кремнием и серой.

Что такое элемент?
В истории до сравнительно недавнего времени элементами считали огонь, воздух, воду и землю. Загадочный пятый элемент — эфир — добавили, чтобы как-то описать состав звезд, поскольку, с точки зрения философа Аристотеля, из земных элементов они состоять не могут. Слово «элемент» происходит от латинского elementum, что означает «первый принцип», или «простейшая форма», — неплохое описание, однако оно все же не объясняет разницу между элементом и простым веществом.
А разница вот в чем. Простое вещество — форма существования атомов определенного химического элемента, а химический элемент — совокупность атомов с одинаковым зарядом ядра. Кусок Брандова фосфора — ядовитого вещества и составляющей одного нервно-паралитического газа, так уж вышло, — состоит из атомов одного химического элемента. Что занимательно, не все куски фосфора выглядят одинаково, потому что атомы фосфора могут быть организованы по-разному, из-за чего меняется не только внутреннее устройство вещества, но и его внешний вид. В зависимости от того, как именно организованы его атомы, фосфор бывает белый, черный, красный или фиолетовый. Эти разновидности и ведут себя по-разному — например, температуры плавления у них сильно разнятся. Белый фосфор плавится на солнце в жаркий день, а черный придется для этого греть до 600 °С в ревущей домне. Хотя и тот и другой состоят из одних и тех же атомов с составом из 15 протонов и 15 электронов.
Закономерности Периодической таблицы
На несведущий взгляд, Периодическая таблица представляется эдакой оригинальной игрой «Тетрис», где, в зависимости от того, на какую версию вы смотрите, те или иные детальки не долетели до дна. На первый взгляд в таблице не мешало бы навести порядок. На самом же деле этот сумбур строго упорядочен, и в кажущемся кавардаке любому химику по силам быстро отыскать нужные сведения. А все оттого, что в этой хитрой схеме содержатся скрытые закономерности, объединяющие элементы в соответствии с их атомным устройством и химическим поведением.
«Мир химических реакций подобен театральной сцене... Актеры – вещества» Клеменс Александр Винклер (1838-1904), немецкий химик-технолог, первооткрыватель элемента германия
Вдоль рядов таблицы слева направо элементы выстроены по порядку атомного числа — количества протонов в ядре атома элемента. Однако гений Менделеева распознал, что свойства элементов с определенного места в таблице начинают повторяться и следует начать новый ряд. Соответственно, из столбцов можно извлечь более подробные сведения о том или ином элементе и его простых веществах. Возьмем столбец (группу) справа, от гелия до радона. Это благородные (инертные) газы, бесцветные и при нормальных условиях чрезвычайно ленивые в отношении каких бы то ни было химических взаимодействий. Неон, к примеру, до того неактивен, что его никак не заставишь создать химическое соединение ни с каким другим веществом. Причина такого безразличия — в электронном устройстве атомов неона. Если представить модель атома упрощенно, внутри любого атома электроны располагаются на определенных концентрических оболочках — и лишь в определенном количестве. Если оболочка уже заполнена, электроны занимают следующий слой, отстоящий от ядра дальше. Поскольку число электронов в атоме возрастает от элемента к элементу по мере увеличения атомного числа, у атома каждого элемента — своя электронная конфигурация. Ключевая особенность благородных газов в том, что их внешние оболочки заполнены. Такая структура очень устойчива, то есть электроны трудно вовлечь в какие бы то ни было взаимодействия.
В Периодической таблице много и других закономерностей. При движении вдоль ряда слева направо, к инертным газам, вырвать электрон из атома делается все труднее (требуется больше энергии); то же верно и при движении снизу вверх. Середина таблицы занята в основном металлами, и по мере приближения к нижнему левому углу они делаются все более металлическими. Применяя понимание этих закономерностей, химики предсказывают, как поведут себя в химических реакциях те или иные простые вещества.
Сверхтяжелые
У химии с боксом мало общего, но одно их роднит: и там и там есть свои чемпионы-сверхтяжеловесы. Те, что «в цыплячьем весе», плавают вверху Периодической таблицы — у атомов водорода и гелия на двоих всего три протона, зато те, что внизу, затонули под тяжестью своего атомного груза. Таблица за многие годы разрослась и включила в себя вновь открытые элементы, все весомее и весомее. Однако номером 92 — радиоактивным элементом ураном — завершается ряд элементов, находимых в природе. И хотя в результате нейтронного захвата с последующим бета-распадом образуется плутоний, его количества в естественных условиях исчезающе малы. Плутоний обнаружили в ядерном реакторе, а другие сверхтяжелые атомы получены столкновением атомов более легких элементов в ускорителях элементарных частиц. Охота еще не закончена, однако в любом случае она теперь намного заковыристее, чем упаривание телесных жидкостей.
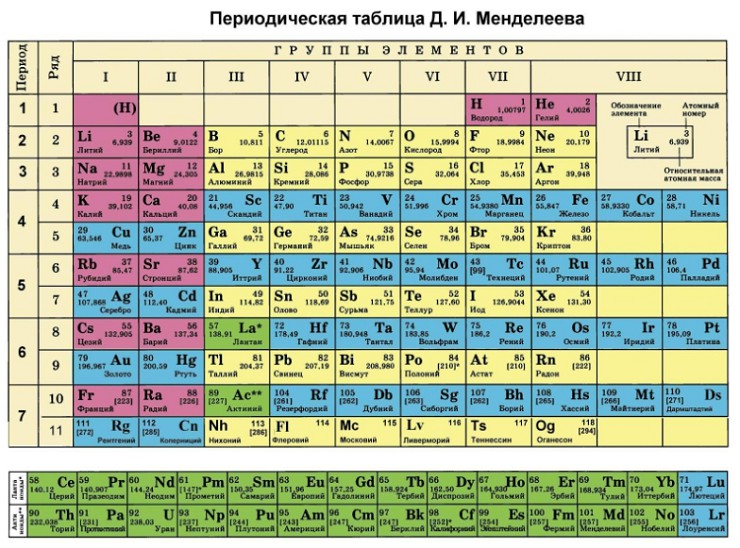
Расшифруем Периодичекую таблицу
В Периодической таблице элементы обозначены буквами. Некоторые аббревиатуры очевидны: например, Na - натрий. Зато другие - допустим, As (мышьяк) - не сразу понятно, откуда взялись. Число над буквой - массовое, оно соответствует числу нуклонов (протонов и нейтронов) в ядре атома этого элемента. Нижний индекс - число протонов (атомное число).
Охота на тяжелейшего среди сверхтяжелых
Жулики не нравятся никому, но они есть в любой профессии, и ученые - не исключение. В 1999 году исследователи из Национальной лаборатории имени Лоренса в Беркли (Калифорния) опубликовали статью, посвященную открытию сверхтяжелых элементов № 116 (ливерморий) и № 118 (унуноктий). Но что-то в той статье не сходилось. Другие ученые, ознакомившись с новостью, попытались повторить представленные калифорнийцами эксперименты, но, как ни старались, им не удалось получить ни единого атома элемента № 116. Оказалось, что один из «первооткрывателей» фальсифицировал данные, в результате чего некоему правительственному агентству в США, профинансировавшему эти исследования, пришлось с позором отказаться от заявлений о прорыве в мировой науке. Статью изъяли, а лавры открытия ливермория достались группе русских исследователей годом позже. Ученого, подделавшего данные, уволили. Вот каков престиж открытия нового элемента в наши дни. Исследователи ради этого готовы ставить на кон всю свою карьеру.
